北方伟业计量集团有限公司
-
登录 |
-
官方微信 |

-
在线支付 |
- 网站地图
- 产品
- 新闻
- 课堂
北方伟业计量集团有限公司









秒表,温度计(0~100℃),碘量瓶(100 m L×9,洁净干燥),吸量管或取液器若干,铜水浴锅(或超级恒温水浴缸),冰块,标签纸,滤纸片,搅拌子,电磁搅拌器。

在室温下,以吸量管(贴标签,专用;或取液器)按照表格中的数据分别量取适量KI、淀粉和Na2S2O3溶液加入碘量瓶中,放入洁净搅拌子并将碘量瓶置于电磁搅拌器上搅拌,使溶液混合均匀。再用另一吸量管(或取液器)量取适量K2S2O8溶液(或Fe Cl3溶液),迅速倒入碘量瓶中,立即计时并将碘量瓶塞盖上,当溶液刚出现蓝色时停止计时,记下时间Δt和室温。
用同样的方法按照表中的数据进行其他实验。为使溶液的总体积和离子强度保持不变,实验中KI、K2S2O8所减少的量分别用等体积、同浓度的KNO3、K2SO4溶液补充,Fe Cl3则以等体积、2倍浓度的Na Cl液补充。
按照各表中实验编号4的试剂用量,将Na2S2O3、KI、KNO3和淀粉溶液加入碘量瓶,将K2S2O8(或Fe Cl3)溶液放入另一个碘量瓶(或小烧杯)中,并同时置入冰水浴(或超级恒温水浴)中冷却(或升温10℃)。待溶液均恒定至预定温度时,把K2S2O8(或Fe Cl3)迅速倒入到KI等的混合溶液中,立即计时加塞,并搅动溶液,当溶液刚出现蓝色时,停止记时,记录反应的时间与温度。
Cu2+可以使K2S2O8与KI的反应速率增大。按表格中实验编号4的试剂用量,将Na2S2O3、KI、KNO3和淀粉溶液加入碘量瓶中,再加入3滴0.020 mol·L-1Cu(NO3)2溶液,摇匀,迅速倒入K2S2O8溶液,在室温下重复上述实验,记录反应时间。
1.(NH4)2S2O8-KI反应体系实验效果分析
将(NH4)2S2O8-KI反应体系的实验数据列表如下,可与另两种反应体系进行实验效果对比,(NH4)2S2O8溶液最好现用现配。
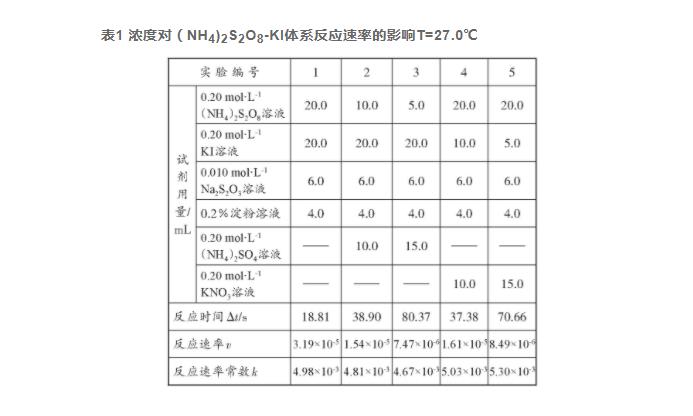
由表1数据可知,该实验体系在27.0℃时的反应速率常数k的相对平均偏差为3.52%。不考虑(NH4)2S2O8溶液在常温下易变质的缺点,该体系的实验结果还是比较令人满意的。
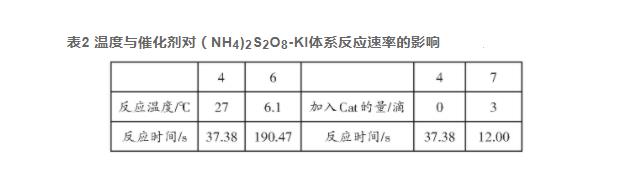
表2为温度与催化剂对(NH4)2S2O8-KI体系反应速率的影响。经计算,在此实验条件下该体系的活化能Ea为55.58 k J∙mol-1,与理论值51.88 k J∙mol-1相比,相对偏差为7.13%。
因K2S2O8与(NH4)2S2O8参与反应的离子一致,反应原理相同,故优先分析K2S2O8-KI反应体系。
将不同反应物浓度、不同反应体积的K2S2O8与KI记为a、b、c、d、e五个组分别进行实验,计算各自的反应速率、反应速率常数及活化能,并分析实验结果。实验以数据准确合理、试剂消耗低、产生废液量少为基本依据,优选出合适浓度与反应体积的实验组别。K2S2O8-KI反应体系实验数据见表3至表9。
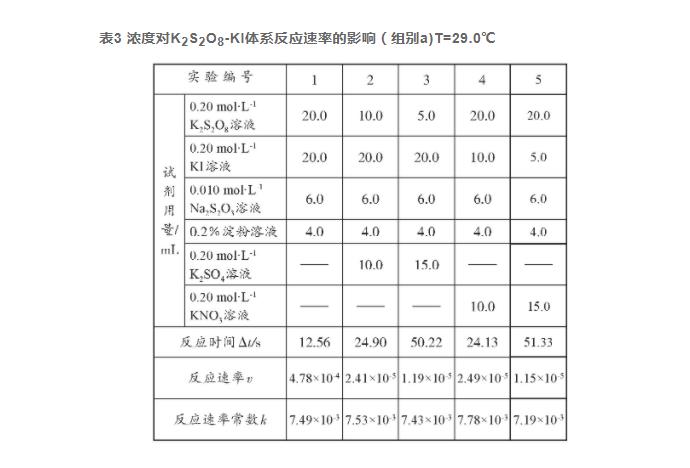
声明:本文所用图片、文字来源《大学教育》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系删除。

由于闽江流域近年频发水质污染突发事件,本文结合实地调研及有关部门内部统计,采用专家分析法开展污染因子调查,采用风险矩阵LS法对污染因子进行定性评价。评价结果为闽江上游入流污染物(突发)、沿线生活污染源(排口污染物)等级较高。为方便进一步风险评估,拟建立二维水动力水质模型进行数值仿真分析。
了解更多> >根据实测调研及相关风险分析,针对3个不同风险点,选取特枯年、平水年、丰水年3种典型代表年作为来流条件,选定污染程度为轻度污染、中度污染、重度污染3种类别,参考GB 8978——1996《污水综合排放标准》、GB3838—2002《地表水环境质量标准》、实地调研确定输入污染。点源污染日排放量设定见表1。排放时间设定7 d和30 d,共54种工况。
了解更多> >污染物整体分布特征。因水体中初始含有一定氨氮,当含有氨氮水体汇入水库中时,由于水库流速较缓,导致取水口附近氨氮大量聚集率先达到较高浓度,上游来流输入氨氮浓度相对水库中氨氮浓度较低,在空间上呈现分布不均的现象。总体分布特征为上游水口电站氨氮浓度低、下游取水泵站及文山里氨氮浓度高,又因受到潮汐作用,文山里的氨氮浓度随时间周期性波动。在潮汐的影响下,污染事件发生2个月后,水库中氨氮浓度仍高于III类水指标限值。
了解更多> >针对闽江竹岐水源地突发水污染事件,需结合应急调控预案预估污染事件发生趋势、确定污染事件造成峰值浓度、允许采取措施的预警时间及其在潮汐作用下最终的波动范围,综合考虑风险等级及预警时间确定污染事件的紧迫性和及时处理的可能性,根据调控目标对泵站取水口进行调控,及时有效地处理水源地突发水污染事件。
了解更多> >现阶段,化学合成添加剂被广泛运用到食品的生产加工过程中,但若化学合成添加剂使用不当就会造成严重的食品安全事件。本文首先阐述了化学合成添加剂的使用现状,然后分析了其对食品安全产生的影响,最后就化学合成添加剂的检测方法进行了研究。
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13803766220,010-58103678
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论