北方伟业计量集团有限公司
-
登录 |
-
官方微信 |

-
在线支付 |
- 网站地图
- 产品
- 帖子
- 新闻
- 课堂
- 文库
北方伟业计量集团有限公司








GC:精密量取对照品储备液0.5、1.0、2.0、4.0、5.0mL分别置于10mL量瓶中,用无水乙醇定容,得标准曲线溶液,按色谱柱:AgilentZORBAXEclipseXDB-C18(4.6x250mm,5μm),流动相为甲醇(A)-20mmo/L乙酸铵溶液(B),梯度洗脱(0~8min,10%A;8.1~20min,30%A;20.1~30min,10%A),流速为1.0mL/min,进样量为10uL,柱温为35℃,检测波长为210nm。HPLC:精密量取对照品储备液0.04、0.4、1.0、1.5、2.0mL分别置于10mL量瓶中,用50%甲醇溶液定容,得标准曲线溶液。
GC-MS:精密量取对照品储备液1mL置10mL量瓶中,加无水乙醇制成浓度为100μg/mL的对照品使用液,再精密量取0、0.4、0.2、0.5、1.0、2.0mL分别置于10mL量瓶中,用无水乙醇定容,得标准曲线溶液,按色谱条件:色谱柱为J&WDB-624UI(60mx0.25mmx1.4μm),升温程序为初始温度60℃,保持1min,以50℃/min升温至150℃,保持2min,再以10℃/min升温至250℃,保持26min;载气为氦气,初始流量1mL/min,保持20min,以2mL/min升至2mL/min,保持20min,进样口温度250℃,分流比10:1,进样量1μL。
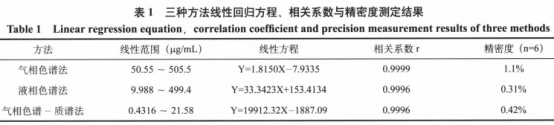
分别以峰面积为纵坐标,浓度为横坐标,得线性回归方程和相关系数,测定结果如表1所示。结果表明,三种方法的相关系数均达到>0.999,且精密度RSD均<2%,表明线性和精密度良好。
精密量取各对照品溶液,以信噪比S/N=3和S/N=10为依据分别制成检出限溶液和定量限溶液,GC、HPLC、GC-MS三种方法的检出限分别5mgkg、10mg/kg和2mg/kg;定量限分别为17mg/kg、33mg/kg和6.7mg/kg。可见,GC-MS的检出限最低,灵敏度相对较高,HPLC的检出限相对较高,灵敏度相对较低。
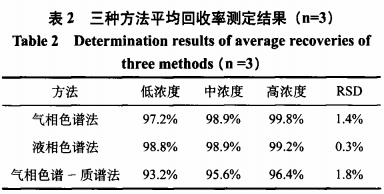
取已知含量的某口服液0.5g各9份,根据曲线范围,按低、中、高浓度分别精密加入各自的对照品储备液(GC加入1、3、5mL,HPLC加入1、2、3mL,GC-MS加入0.1、0.3、0.5mL),每个浓度3份,按各自的溶液制备方法制备回收率溶液,三种方法的回收率测定结果如表2所示。结果表明,三种方法的回收率均在90%~100%之间,方法的准确性良好。
取三种方法制备的标准曲线中点浓度溶液和回收率考察的样品溶液,在室温条件下,分别于0、0.5、1、2、4、8、16、24h时在各自的色谱条件下测定,计算各时间点苯甲醇峰面积的RSD%。GC为1.1%、1.3%,HPLC为0.8%、0.9%,GC-MS为1.4%、1.3%,均小于2%,表明三种方法在室温下具有良好的稳定性,能满足日常检验的需求。
依据GB5009.28-201方法,取含蛋白质的样品1.0g,加入适量的苯甲醇标准物质,再加入92g/L亚铁氰化钾和183g/L乙酸锌溶液各0.5mL后,精密称取苯甲醇对照品25mg置于10mL量瓶中,加50%甲醇溶液稀释并定容,得对照品储备液。取样品混匀,精密称取1.0g置于25mL量瓶中,加适量50%甲醇溶液超声提取10min,冷却至室温后定容,0.22μm滤膜滤过,得样品溶液高效液相色谱法项下制备样品溶液并测定含量,并与未加入蛋白质沉淀剂的加标样品溶液测定结果进行比较。结果表明,蛋白质沉淀剂对苯甲醇的测定无影响。
依据GB5009.139-2014方法,取含苯甲醇的样品1.0g,置于25mL量瓶中,加适量50%甲醇溶液超声提取10min后定容至刻度,再加入0.5g轻质氧化镁混匀,0.22μm滤膜滤过后按色谱柱:AgilentZORBAXEclipseXDB-C18(4.6x250mm,5μm),流动相为甲醇(A)-20mmo/L乙酸铵溶液(B),梯度洗脱(0~8min,10%A;8.1~20min,30%A;20.1~30min,10%A),流速为1.0mL/min,进样量为10uL,柱温为35℃,检测波长为210nm色谱条件测定含量,并与未加入氧化镁的样品测定结果进行比较。结果表明,轻质氧化镁对苯甲醇的测定无影响。
依据GB5009.140-2003方法,取含苯甲醇的样品1.0mL,置于中性氧化铝(100~200目)柱中,用50%甲醇溶液洗脱至25mL容量瓶中,0.22μm滤膜滤过后测定含量,并与未过中性氧化铝柱的样品测定结果进行比较。结果表明,中性氧化铝柱对苯甲醇的测定无影响。
收集市售的40批液体型保健食品,精密称取苯甲醇对照品50mg置于50mL量瓶中,加无水乙醇稀释并定容,得对照品储备液。取样品混匀,精密称取1.0g,置于10mL量瓶中,加无水乙醇溶解并超声提取10min,冷却至室温后定容,0.22μm滤膜滤过,得样品溶液。精密称取苯甲醇对照品25mg置于10mL量瓶中,加50%甲醇溶液稀释并定容,得对照品储备液。取样品混匀,精密称取1.0g置于25mL量瓶中,加适量50%甲醇溶液超声提取10min,冷却至室温后定容,0.22μm滤膜滤过,得样品溶液。对照品储备液同气相色谱法项下储备液。取样品混匀,精密称取1.0g,置于10mL量瓶中,加无水乙醇溶解并超声提取10min后定容,0.22μm滤膜滤过,精密量取续滤液0.1mL置于10mL量瓶中,加无水乙醇定容,得样品溶液。
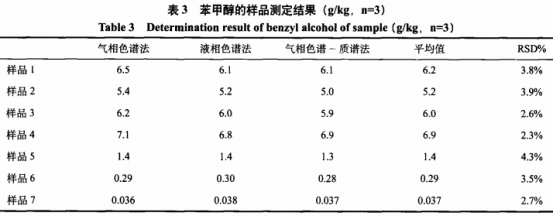
在色谱柱:J&WDB-WAX(60mx0.25mmx0.25μm),升温程序为初始温度150℃,10℃/min升到180℃,保持3min,20℃/min升到230℃,保持5min;载气为氮气,恒流速度1.0mL/min,分流比10:1,检测器温度250℃,进样口温度240℃,进样量1μL。色谱柱:AgilentZORBAXEclipseXDB-C18(4.6x250mm,5μm),流动相为甲醇(A)-20mmo/L乙酸铵溶液(B),梯度洗脱(0~8min,10%A;8.1~20min,30%A;20.1~30min,10%A),流速为1.0mL/min,进样量为10uL,柱温为35C,检测波长为210nm。色谱条件:色谱柱为J&WDB--624UI(60mx0.25mmx1.4μm),升温程序为初始温度60℃,保持1min,以50℃/min升温至150℃,保持2min,再以10℃/min升温至250℃,保持26min;载气为氦气,初始流量1mL/min,保持20min,以2mL/min升至2mL/min,保持20min,进样口温度250℃,分流比10:1,进样量1μL条件下测定,根据苯甲醇标准曲线范围调整样品的稀释体积,结果表明,有7批样品检出含苯甲醇,三种方法的测定结果一致(见表3),相对标准偏差均小于5%。
GC是测定挥发性或半挥发性成分的首选方法,其灵敏度好,进样量小,检测效率较高,检测成本低,但是仅采用保留时间定性,当样品中有杂质干扰时,需要调整升温程序实现最佳分离效果。
HPLC是实验室最普及的检测手段,在测定苯甲醇含量时,可以根据光谱图进行定性判定,但由于苯甲醇的最大吸收波长在210nm附近,属末端吸收,没有明显的吸收特征,当有杂质干扰时,可能会影响判定的准确性。但从本文的测定结果看,本方法与测定波长相近的10-羟基癸烯酸等功效性指标的分离度很高,受杂质干扰较少。
GC-MS相比前两种方法,其灵敏度最高,根据质谱图定性判定,并可准确定量,但仪器使用和维护成本较高,推荐作为GC和HPLC的辅助判定方法。
本文建立的三种苯甲醇测定方法操作简单,准确性高,稳定性好,实验室可根据条件选择适宜的检验方法。三种方法相比,推荐使用HPLC法进行测定,GC-MS法辅助判定,也可直接采用GC-MS法,提高监测效率。
《保健食品备案产品可用辅料及其使用规定(2019年版)》中规定的苯甲酸及其钠盐在液体制剂中的最大使用量为1g/kg;在GB/T2731-2017《日用香精》1161中规定,苄醇(即苯甲醇)在第1类加香产品(唇用产品、玩具)中,最高限量为0.2%(即2g/kg);根据JECFA提出的苄基化合物的总使用限值要求0~5mgkg体重(以苯甲酸当量计),以成年人体重60kg计算,苯甲酸类ADI为0~300mg/d这几个标准均可作为制定食品或保健食品中苯甲醇限量的参考依据。
声明:本文所用图片、文字来源《中国食品添加剂》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系

由业伟计量和安省徽环境测检行业会协共同举办的《安省徽实验质室量控与制环境监技测术交流会》将于10月28日在合肥隆召重开,行业家专大咖齐聚,实室验人员费免参会习学交流,报名礼有先到先得哦!
了解更多> >不平凡的2020年已经结束,我们见证了乘风破浪、生命至上,也学会了勇敢攀登、迎难而上。回望这特殊的一年,想必每个伟业人心中都充满回忆,让我们共同回忆这些难忘的的画面,伴你温暖前行。
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13803766220,010-58103678
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论