北方伟业计量集团有限公司
-
登录 |
-
官方微信 |

-
在线支付 |
- 网站地图
- 产品
- 帖子
- 新闻
- 课堂
- 文库
北方伟业计量集团有限公司








可食用动物加工成食品后,在养殖过程中使用的兽药有可能会有残留,如抗生素、抗菌剂等。SHARMA等人利用AuNPs类过氧化物酶活性和Ky2适配体构建“turn-off/turn-on”传感器,实现了卡那霉素的高灵敏快速检测,检测限1.49nmol/L,时间3~8min,比传统的盐诱导AuNPs聚集方法灵敏15倍,速度快20倍。WANG等人发现卡那霉素通过-NH2吸附在柠檬酸盐封端的AuNPs上,改变AuNPs表面性质,从而增强AuNPs的过氧化物酶活性;基于此原理,开发了基于AuNPs过氧化物酶活性变化直接检测卡那霉素的方法,方法简便,不需要对AuNPs进行任何修饰,在奶、肉中检测限低至0.1nmol/L。ZHAO等人以ABTS为显色底物构建AuNPs-适配体传感器检测牛奶中的链霉素,线性范围0.1~0.5μmol/L,检测限86nmol/L。类似地,SONG等人发现带负电的诺氟沙星通过静电相互作用吸附在带正电荷的1-Me-D-Trp@AuNCs(1-甲基-D-色氨酸修饰的纳米金簇)表面,提高1-Me-D-Trp@AuNCs的酶活性,无需适配体即可直接检测诺氟沙星,检测限0.2μmol/L。ZHANG等人发现四环素的特异性适配体增强AuNPs酶活性,而加入四环素时,AuNPs酶活性降低,以此实现原料奶中四环素的高灵敏度检测,该方法检测限为46nmol/L。
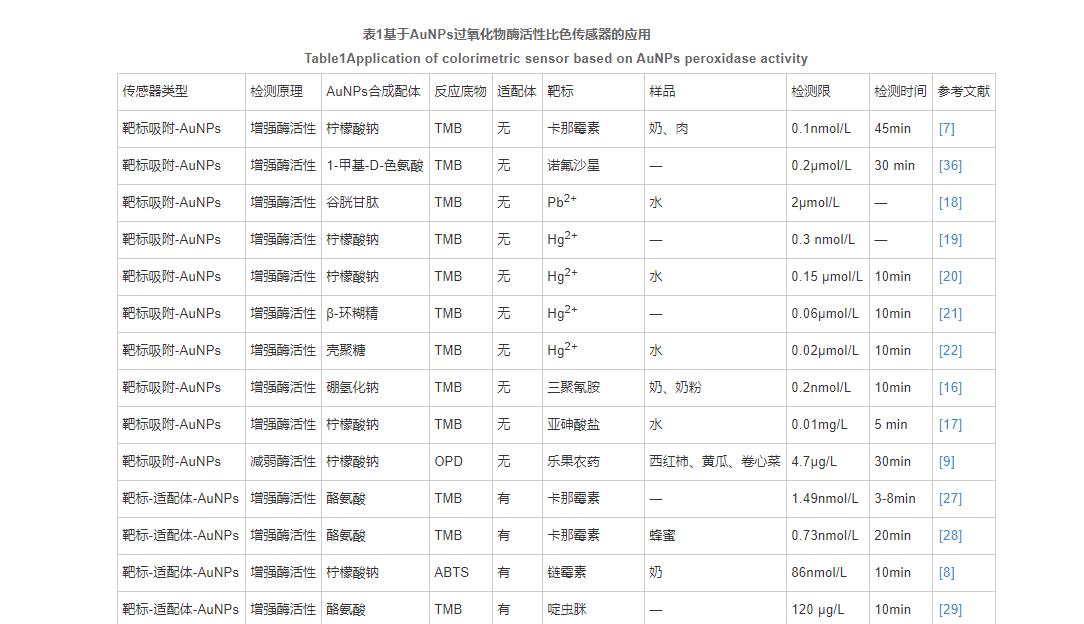
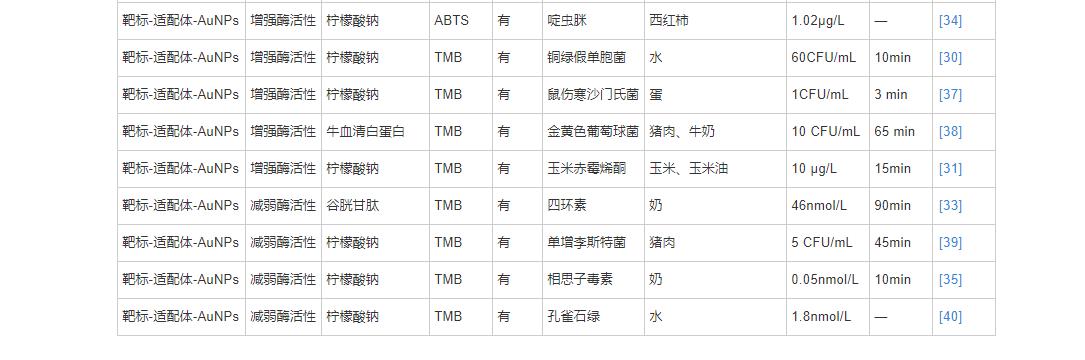
环境中的重金属元素可能通过食物链转移至人体,危害人类身体健康。LIAO等人利用Pb2+诱导AuNPs聚集,增强其过氧化物酶活性的原理,建立了一种简单可靠的比色方法,用于检测水中的Pb2+含量。LONG等人发现Hg2+可被AuNPs表面的柠檬酸钠还原为Hg0,Hg0分散在AuNPs表面,改变表面性质,提高AuNPs的过氧化物酶活性,从而无标记检测Hg2+。HAN等人的研究证实了LONG的观点,并且制成了AuNP比色试纸条,能同时执行多个样品检测,简单便携,可应用于现场检测。An等人在LONG的比色传感体系的基础上,使用温度计作为信号读取器,当加入Hg2+时,AuNP@β-CD(β-环糊精修饰的纳米金)的催化活性显著提高,蓝色oxTMB的形成增强,从而导致温度升高,可以在10min内快速检测,检测限0.06μmol/L。JIANG等人用生物相容性更高的壳聚糖纳米金(CS-AuNPs)检测水中的Hg2+,检测限为0.04μmol/L。
蔬菜、水果、谷物等农作物表面易残留种植过程中施用的农药。HU等人发现乐果农药的分子结构中含有酰胺键,可能起着与巯基相似的作用,能螯合Au+来抑制AuNPs的酶活性,因此可用AuNPs检测黄瓜、西红柿、卷心菜等农产品中的乐果农药,检测限为4.7 μg/L。WEERATHUNGE和YANG利用啶虫脒与适配体结合从而恢复AuNPs酶活性,分别以TMB和ABTS为显色底物,开发了检测啶虫脒的适配体-AuNPs传感器,各自的检测限分别为120 μg/L和1.02μg/L。
食源性致病菌直接或间接污染食品及水源,是导致食品安全问题的重要来源。DAS等人利用铜绿假单胞菌与其适配体的结合恢复AuNPs的酶活性构建传感器,可以在10min内完成快速检测,检测限为60CFU/mL。CHEN等人也基于此原理建立了鼠伤寒沙门氏菌的检测方法,在鸡蛋样品中检测限低至1CFU/mL。YAO等人选择金黄色葡萄球菌免疫球蛋白Y(IgY)作为适配体,适配体修饰抑制了AuNPs催化活性,金黄色葡萄球菌的结合恢复AuNPs酶活性,催化TMB底物显色。该方法对复杂食品基质中金黄色葡萄球菌的定量检测具有很强的抗干扰能力,在猪肉、牛奶中检测限为10CFU/mL,但检测时间较长,需要65 min。陈威风等人发现单增李斯特菌的适配体增强AuNPs酶活性,单增李斯特菌与适配体特异性结合使AuNPs酶活性降低,从而检测猪肉中的单增李斯特菌,检出限约为5 CFU/mL。
NI等人利用三聚氰胺使AuNPs过氧化物酶活性增强的原理简便快速地检测原料奶和奶粉中的三聚氰胺,检测限为0.2nmol/L。基于相似的原理,XUE等人建立了亚砷酸盐的检测方法,检测限为0.01mg/L。SUN等人报道了一种基于适配体的比色检测法玉米赤霉烯酮(ZEN),适配体抑制AuNPs酶活性,在ZEN存在的情况下,适配体与ZEN结合,不再抑制AuNPs酶活性,此方法可在15min内快速响应,检测限为10ng/mL。而HU等人报道的相思子毒素(Abrin)检测原理则刚好相反,Abrin的适配体活化AuNPs表面提高酶活性,Abrin结合导致适配体从AuNPs表面脱附,导致酶活性降低。ZHAO等人用CATB修饰AuNPs,适配体抑制CATB-AuNPs的酶活性,加入孔雀石绿后,酶活性恢复,此方法检测限低至1.8nmol/L。
不难发现,目前基于酶活性的适配体-AuNPs比色传感器的核心原理是靶标结合适配体使其从AuNPs上解吸附,从而调控酶活性。这种解释基于一个假设前提:靶标与适配体结合的亲和力远大于适配体与AuNPs的结合力,只考虑到靶标与适配体的结合,而忽略了靶标与AuNPs之间潜在的相互作用。最近的一些研究表明,靶标仅能解吸下来极少的预先吸附的适配体(解吸率<5%),也就是说几乎不可能通过靶标-适配体结合从AuNPs表面解吸适配体;同时,靶标可以吸附在AuNPs上,并且抑制适配体的吸附。因此AuNPs酶活性的调控可能不依赖于靶标-适配体的结合,而是取决于靶标与AuNPs的吸附。如前文所述,SHARMA等人用适配体-AuNPs检测卡那霉素,认为卡那霉素通过特异性结合使适配体解吸,从而增强AuNPs酶活性。但根据ZHOU等人的报道,卡那霉素很难使适配体从AuNPs表面解吸(卡那霉素浓度为10 μmol/L时,适配体几乎没有解吸,浓度高达0.1 mmol/L时只有12%适配体解吸,而浓度再升高并没有引起更多的适配体解吸);同时,WANG等人发现卡那霉素通过静电吸引和氨基-羧基相互作用强吸附在柠檬酸盐包被的AuNPs表面。因此AuNPs酶活性的增强很可能归功于卡那霉素在AuNPs上的吸附,而不是适配体从AuNPs表面解吸。
因此我们在讨论靶标-适配体-AuNPs比色传感的原理时,务必要考虑AuNPs对靶标的吸附情况。对于AuNPs弱吸附的靶标,如K+,可以用靶标-适配体结合使适配体从AuNPs解吸,从而调控AuNPs酶活性来解释。但对于强吸附的靶标,如卡那霉素、氯霉素、亚砷酸盐、ATP、多巴胺等,这种原理解释只有部分正确。为了更严谨地解释,可以引入一段适配体的非结合突变序列作为对照,或者对AuNPs进行表面修饰使其对靶标的吸附力减小。
基于AuNPs过氧化物酶活性构建的比色传感器已经在应用方面取得了很多优秀的成果,但仍然面临一些亟待解决的问题,如下:
(1)吸附在AuNPs上的靶标分子如何调节AuNPs的酶活性,还有待系统地研究。
(2)提高AuNPs在中性条件下的酶活性。AuNPs的最佳催化活性一般发生在强酸性条件下(pH值在3~4左右),中性条件下的过氧化物酶活性可以忽略不计。这一缺点导致AuNPs无法应用于某些需要中性pH条件的靶标(如蛋白质),因为蛋白质在强酸性环境中会发生构象变化,可能导致检测的准确性和灵敏度变差。
(3)基于AuNPs酶活性构建的比色传感器,绝大多数利用的是AuNPs过氧化物酶性质,其他酶性质的利用还有待开发,期待未来创造更多的响应信号类型。
声明:本文所用图片、文字来源《食品与发酵工业》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系删除。

本次推荐的有两场展会,6月3-4日CBIFS2021第十四届中国国际食品安全技术论坛,6月17-19日第十八届南京科学仪器及实验室装备展览会快看看有没有您关注的展会吧,伟业计量也将为您持续推荐,敬请关注!
了解更多> >随着经济社会的发展,人们的物质生活水平得到极大的提升,食品安全问题也日益突出。目前,各种食品安全问题时有发生,如“地沟油”“染色馒头”等,严重威胁人们的生命健康。人们要认识到问题的严重性,针对当前食品安全所存在的问题有针对性建议,更好地保障食品安全,促进社会和谐稳定发展。
了解更多> >随着技术的不断发展,转基因食品在不断增多。目前,转基因食品的安全问题仍存在争议,由此我国研发了转基因食品检测技术。转基因快速检测技术可对食品酶活性、酸及蛋白等指标进行检测,如果检测符合正常指标规定,即可放心食用。
了解更多> >食品在加工、运输、储存等过程中有可能带入有害物质,如兽药残留、重金属残留、农药残留、致病菌等,对食品质量安全造成威胁,因此有必要探索准确、高效、灵敏、经济的检测方法以保障消费者的食品安全。传统的食品安全检测方法如气相色谱法、高效液相色谱法等虽然准确性高,但是步骤繁琐、成本高、耗时长、需在实验室进行,不能实现高效、现场检测。近年来,随着纳米技术的发展,许多基于纳米材料的智能传感器在检测中得到广泛应用。
了解更多> >可食用动物加工成食品后,在养殖过程中使用的兽药有可能会有残留,如抗生素、抗菌剂等。SHARMA等人利用AuNPs类过氧化物酶活性和Ky2适配体构建“turn-off/turn-on”传感器,实现了卡那霉素的高灵敏快速检测,检测限1.49nmol/L,时间3~8min,比传统的盐诱导AuNPs聚集方法灵敏15倍,速度快20倍。
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13803766220,010-58103678
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论