北方伟业计量集团有限公司
-
登录 |
-
官方微信 |

-
在线支付 |
- 网站地图
- 产品
- 帖子
- 新闻
- 课堂
- 文库
北方伟业计量集团有限公司








由新型冠状病毒(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)导致的新型冠状病毒肺炎(corona virus disease 2019, COVID-19)自2019年肆虐全球,给人类带来了重大的生物安全威胁。COVID-19主要通过呼吸道飞沫、密切接触以及气溶胶等途径传播,传染性强、传播速度快、流行范围广,已导致全球210多个国家和地区暴发疫情。如何预防新冠病毒以及治疗感染患者,对全球公共卫生是一个巨大的挑战。
目前全球都在积极开展药物研发,但针对COVID-19的特效药尚未研发成功,“老药新治”是快速控制疫情的一种有益手段,“老药”相比于全新结构药物,其合成工艺成熟、安全性和药代动力学数据已知,和新药相比有一定的优势。法维拉韦(favipiravir,又称法匹拉韦,图1)是一种新型广谱抗RNA病毒药物,新近的体内外研究证实它对SARS-CoV-2有明确的抑制作用。法维拉韦于2014年3月在日本批准上市,由富士胶片集团富山化学工业株式会社开发,作为日本的国家战略储备药物,被纳入《日本新型冠状病毒疾病治疗方案》。2016年6月,浙江海正药业股份有限公司与日本富山化学工业株式会社签订化合物专利独家授权协议,负责含法维拉韦的抗流感病毒药物在中国的研发、制造与销售。2020年2月15日,由海正药业生产的法维拉韦获国家药品监督管理局有条件批准上市,剂型为片剂,商品名为Avigan®,适应证为治疗成人新型或复发流感(仅限于其它抗流感病毒药物治疗无效或效果不佳时使用)。2020年2月在深圳市第三人民医院进行临床试验,比较了法维拉韦(35例)与洛匹那韦/利托那韦(45例)治疗COVID-19的疗效,结果表明法维拉韦的抗病毒疗效优于洛匹那韦/利托那韦,副作用较低,法维拉韦已被纳入《军队支援湖北医疗队新型冠状病毒感染疾病诊疗方案》。2020年在工信部统一调拨下,海正药业生产的法维拉韦片已经驰援全球26个国家或地区,用于协助治疗COVID-19。
目前美、欧、日、中四国药典均未收载法维拉韦,为了有效控制产品质量,满足企业注册上市及生产的需要,亟需制备法维拉韦首批国家化学对照品。本研究对法维拉韦进行了结构确证,然后针对其特性进行了理化性质检查、纯度分析以及稳定性考察,采用质量平衡法赋值,并通过氟核磁共振定量法、进口对照品外标法及差示扫描量热法对定值的结果进行验证,最终建立了法维拉韦首批国家化学对照品。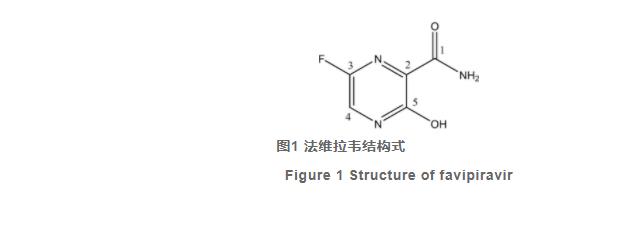
三重四级杆液相质谱仪(Quattro Premier XE QQQ,Waters公司)、核磁共振仪(Bruker Ascend 600,Bruker公司)、5 mm PABBO探头、试验控制及数据处理软件(Topspin4.0,Bruker公司)、傅立叶红外光谱仪(Frontier,PerkinElmer公司)、高效液相色谱仪(e2695-2998,Waters公司)、气相色谱仪(7890B-7697A,Agilent公司)、电子天平(XP205,Mettler公司)、超声仪(KQ-500DB,昆山市超声仪器有限公司)、酸度计(S40K,Mettler公司)、水分测定仪(V30S,Mettler公司)、马弗炉(FP311C,yamato公司)、动态蒸气吸附仪(DVS advantage,SMS公司)、恒温恒湿箱(HPP260,Memmert公司)、差示扫描量热仪(DSC3,Mettler公司)。
法维拉韦待标品(海正药业),法维拉韦进口对照品(批号3812-027A1,TLC公司),法维拉韦杂质Ⅰ~Ⅴ(海正药业),甲醇(批号191614,Fisher公司,含量为99.9%),氘代二甲基亚砜(批号STBJ0941,Sigma公司),溴化钾(批号20160307,国药集团化学试剂有限公司),乙腈(批号JB091230,Merck公司),磷酸二氢钾(批号20181209,国药集团化学试剂有限公司),磷酸(批号20171026,国药集团化学试剂有限公司),无水碳酸钠(批号20170106,国药集团化学试剂有限公司),N,N-二甲基乙酰胺(批号18210305G901,Oceanpak公司),Composite-5卡氏试剂(批号I1710,Fluka公司),4,4’-二氟二苯甲酮(批号:H7H4B-ND,TCI chemicals公司),去离子水(18.2 MΩ,实验室自制)。
质谱离子源为电喷雾离子源(ESI),正离子模式检测,离子源温度120 ℃,毛细管电压3.5 kV,锥孔电压10 V,锥孔气流量50 L/h,脱溶剂气温度350 ℃,脱溶剂气流量600 L/h,流动相为甲醇-水(50:50),流速0.2 mL/min。待标品的质谱图如图2所示,加氢、加钠的准分子离子峰分别为157.86、179.86,与法维拉韦的理论相对分子质量157.10一致。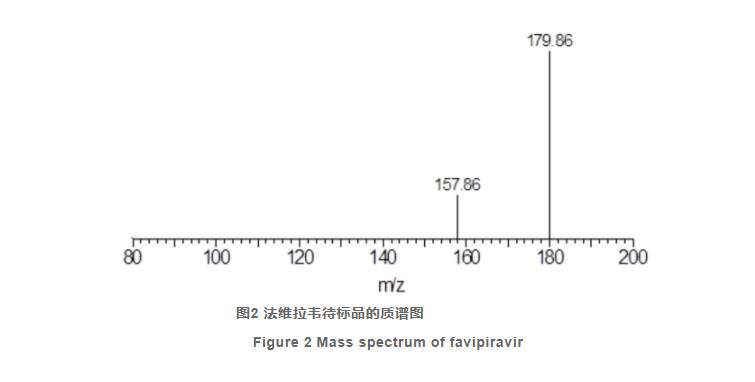
将待标品溶解于氘代二甲基亚砜制成溶液,于600 MHz核磁共振仪中分别测定本品的氢谱和碳谱,见图3。
声明:本文所用图片、文字来源《中国药物警戒》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系删除。

LC-20AD型高效液相色谱仪,配有LC-20AD型紫外可见光度检测器(日本岛津公司);Elmasonic P 60H型超声仪(德国Elmasonic公司,功率为320 W,频率为80 k Hz);XS-105型电子分析天平(梅特勒-托利多仪器有限公司,精度为十万分之一);BINDER PD60型电热干燥箱(德国Binder公司)。
了解更多> >由新型冠状病毒(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)导致的新型冠状病毒肺炎(corona virus disease 2019, COVID-19)自2019年肆虐全球,给人类带来了重大的生物安全威胁。COVID-19主要通过呼吸道飞沫、密切接触以及气溶胶等途径传播,传染性强、传播速度快、流行范围广,已导致全球210多个国家和地区暴发疫情。如何预防新冠病毒以及治疗感染患者,对全球公共卫生是一个巨大的挑战。
了解更多> >采用溴化钾压片法制样,扫描次数为32,分辨率为4.000,经傅立叶变换红外光谱仪扫描,待标品的红外光吸收图谱与法维拉韦TLC进口对照品的红外图谱一致,见图4。主要特征峰均符合法维拉韦的特征吸收峰,其中3 353.5 cm-1和3 226.3 cm-1为酰胺基N-H伸缩振动吸收峰,1 658.5 cm-1为酰胺基弯曲振动吸收峰,1 672.4 cm-1为酰胺C=O伸缩振动吸收峰,1 437.7 cm-1为酰胺C-N伸缩振动吸收峰;1 561.3 cm-1和1 468.2 cm-1为芳环骨架伸缩振动
了解更多> >温度25℃,氮气体积流量200 mL/min,相对湿度以10%的变化步进,从20%逐渐增加到80%,之后再逐渐降低到20%,dm/dt模式,即达到平衡后自动进入下个湿度。设定自动测定样品质量时间间隔为5 s,自动记录样品质量时间间隔为1 min。法维拉韦的水分吸附动力学曲线见图7,随着环境相对湿度由低到高又由高到低的整个过程,法维拉韦相对质量变化始终小于0.1%,说明待标品不具引湿性,暴露在一定湿度环境中时既不会吸水又不会脱水。
了解更多> >法维拉韦首批国家对照品研制中,采用了质量平衡法、氟核磁共振定量法、进口对照品外标法以及差示扫描量热法4种不同原理的含量测定方法测定了对照品的含量,结果分别为99.7%、99.0%、100.7%、99.8%。由于质量平衡法是WHO推荐的药品标准物质定值方法,能够更准确地反映本品的真实含量,因此该批对照品以质量平衡法的结果进行赋值。研制得到的法维拉韦首批国家对照品具备纯度高、量值准确、稳定性好的特性。
了解更多> >通话对您免费,请放心接听
温馨提示:
1.手机直接输入,座机前请加区号 如13803766220,010-58103678
2.我们将根据您提供的电话号码,立即回电,请注意接听
3.因为您是被叫方,通话对您免费,请放心接听

登录后才可以评论